串联蓄电池组抽头供电问题的研究
5.2 极化过程
充电过程中极板发生三种极化过程:
欧姆极化、电化学极化、浓度差极化。
欧姆极化:充电过程中电子从阳极经过外部导线移动到阴极;同时,溶液中也存在正负离子定向移动,溶液中的离子需要克服极板、电解液、电池隔板的阻力,这种阻力形成蓄电池的欧姆极化内阻。欧姆极化电压符合欧姆定律:UΩ=I*RΩ,充电过程蓄电池电极的发热量符合焦耳定律:
Q=I2RΩt.
电化学极化:充电器向极板输送电荷速度大于极板上的电化学反应速度,来不及参加反应的电荷驻留在极板上,使得阳极板电势向正向偏离,阴极板电势向负向偏离。电化学极化电压理论上为:U1=(RT/nF)*Ln(I/Io)。
浓度差极化:两个极板的充电反应都会产生硫酸,将导致极板附近的硫酸浓度升高,不能很快的扩散,反应产物来不及移除,抑制了反应的速度,需要等到极板附近的硫酸分子扩散开,反应速度才能恢复。因此,充电过程中,充电器也需要克服浓度差极化电压:U2=(RT/nF)*Ln(Id/(Id-I))。
根据对蓄电池的充电和极化过程的分析可以得出如下结论:充电时,充电器需要克服蓄电池极板开路电压和极化电压,充电电压U=ES+ΔU.其中ΔU为欧姆极化电压、电化学极化电压以及浓度差极化电压之和。
6.铅酸蓄电池充电过程中极化电压动态分析
充电时,蓄电池的极化电压是动态变化的。如14V恒压充电器对单个的11V蓄电池充电,如图4所示,充电电压器电压U=ES+ΔU,充电初始时刻,极化电压为3V,浓差极化电压占主导。因为初始时刻,溶液中的硫酸浓度低,反应速度快,在极板附近迅速产生高浓度的硫酸,高的浓差极化电压;随着充电持续进行,蓄电池的电量变大,电池的电动势ES增大,极化电压ΔU逐渐减小,当充电完成后,蓄电池电动势ES为12.6V,极化电压为1.4V,此时硫酸的浓度不再变化,极板的充电反应也已经完成,所以,不存在浓度差极化和电化学极化。
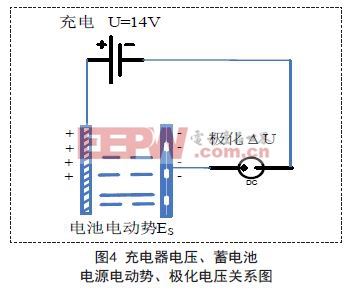
此时,极板的电化学反应不是有效充电的电化学反应,而是水的电解反应,阳极析出O2,阴极析出H2,ΔU为溶液中离子定向移动欧姆电阻引起的电压。电化学反应方程式如下:
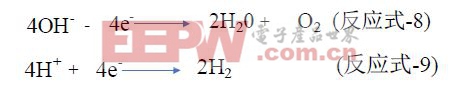
能斯特方程可以证明,蓄电池充电时,发生充电反应极板的电位高于析气电解反应极板的电位。正是由于极化的作用,铅酸蓄电池充电时,由于极板电位的偏移,本应该是析气的电解反应,变成了带极化作用的充电反应。当蓄电池电量充电完成,硫酸扩散完成,极化作用消失,充电反应变成析气的电解反应。
当用一个U=26V的恒压充电器对电量严重不均匀的两节串联电池组充电时,对放电量较大的蓄电池充电无效。
实验数据如下:第一节蓄电池的放电量10%,测得开路电压ES1=12.4V;第二节蓄电池放电80%,测得开路电压ES2=11.2V.实验测得两节电池的极板电压严重不均衡,第一节蓄电池分得充电器14.7V的电压,而放电量80%的蓄电池得到充电电压仅仅只有11.3V;如图5所示。
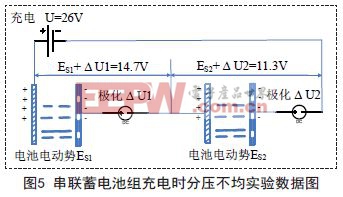
这是因为两节电池串联,充电电流相等;充电初始时刻,由于第一节蓄电池极板只有少量硫酸铅覆盖,所以充电的电化学反应速度快,极板附近的硫酸浓度高,产生较高的浓差极化电压ΔU1;而第二节电池极板被大量的硫酸铅覆盖,反映速度慢,产生较低的浓差极化电压ΔU2;经过多次正反馈,到达平衡状态后,ΔU1≈U-(ES1+ES2),ΔU2≈0,放电量大的蓄电池并没有发生极化,其极板只是产生了析气的电解反应。
通过蓄电池充电过程中极化电压动态分析,可以得出如下结论:恒压充电器对两节串联蓄电池组充电时,如果两节蓄电池放电量严重不均衡,放电量大的蓄电池充电无效。
7.结论
在机动指挥通信系统中,设计人员对机动车两节电池组中间抽头,采用了后节蓄电池12V,提供集群电台的电源,这样的设计将导致后节蓄电池放电量大,引起汽车引擎发电机无法对蓄电池组进行有效的充电,最终导致蓄电池失效。
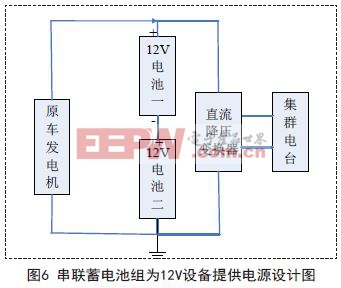
正确的设计方式:取消电池组中间抽头设计,增加一台24V转12V的直流降压变换器,然后再给12V负载供电,如图6所示。




评论